
nProfiler® 1의 위암 예후예측 유전자 분자진단 기술은 위암 환자에 특이적인 유전자들에 대한 분자생물학적 특성에 기반한 기술이기에,
현행의 2기 및 3기 환자 뿐만 아니라 위암 1기와 4기 환자에게도 적용할 수 있도록 다양한 임상시험을 설계 및 진행 중입니다.
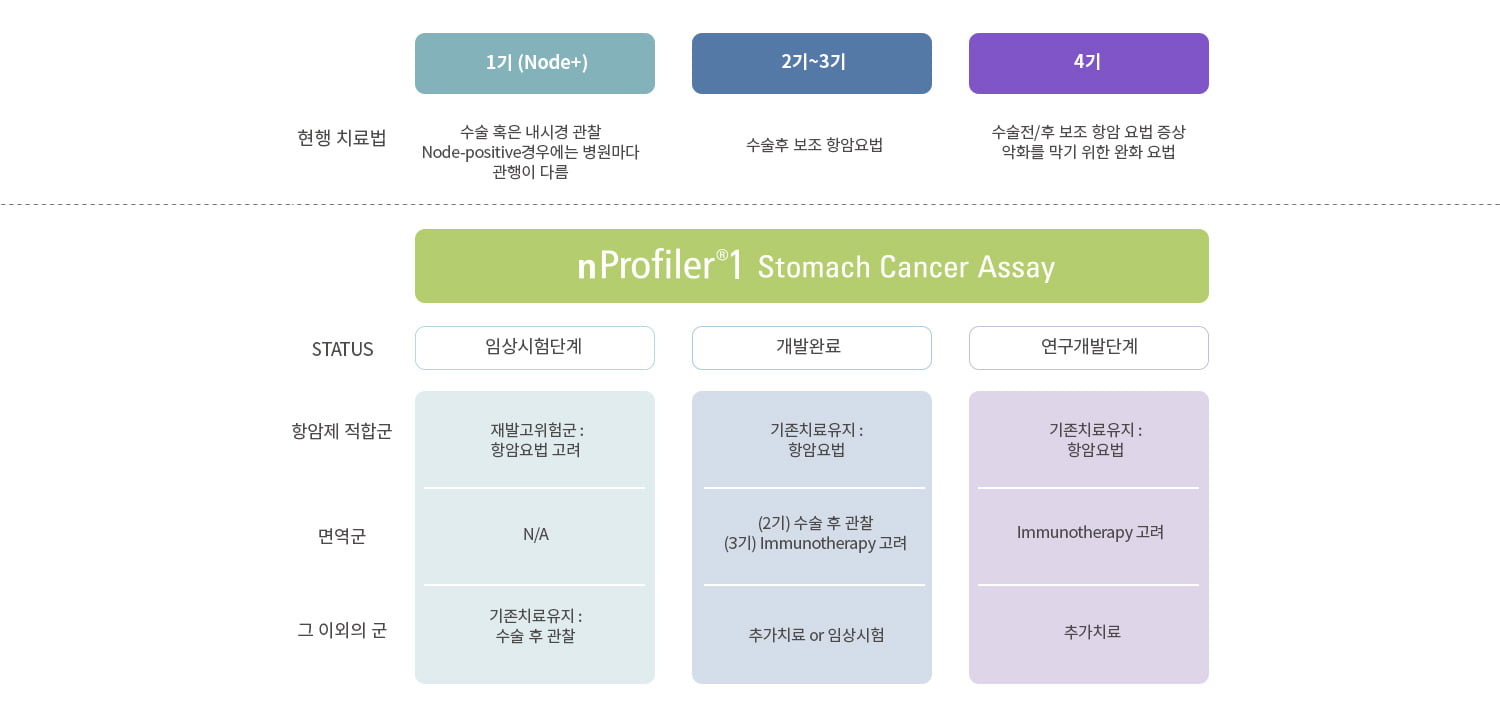
 위암 1기 환자의 항암생존편익 효과 예측 검사
위암 1기 환자의 항암생존편익 효과 예측 검사
최근 국가 암 검진 사업 지원 및 건강 검진이 활발히 이루어짐에 따라 조기 위암의 진단 비율이
증가하고 조기 위암 수술 건수도 증가하고 있습니다.
조기 위암은 진행성 위암과 달리 수술 후 보조항암요법을 받지 않아도 5년 생존율이 90% 이상에
이르기 때문에 흔히 완치가 가능한 질병으로 인식되고 있습니다. 그러나 1기 위암 환자 중에도
재발하는 경우가 종종 있으며, 재발하는 환자는 다발성 전이를 일으키는 등 그 예후가
매우 나쁜 것으로 알려져 있습니다.
특히 림프절 전이가 있는 경우에는 재발율(7.2% ~10.7%)이 림프절 전이가 없는 경우의
재발율(0.6%~1.1%)과 비교해 높아지게 됩니다.
|
Table 1.
Recurrence rate of early gastric cancer according to 6th stage TNM in Seoul National University Hospital (n=1,447) |
||||
|---|---|---|---|---|
| NO | N1 | N2 | Total | |
| T1a | 2/700 0.29% |
1/24 4.17% |
2/8 25.0% |
5/732 0.68% |
| T1b | 5/555 0.90% |
5/140 3.57% |
6/20 30.0% |
16/715 2.24% |
| Total | 7/1255 0.56% |
6/164 3.66% |
8/28 28.6% |
21/1,447 1.45% |
조기 위암 환자의 T, N, M stage별 재발율
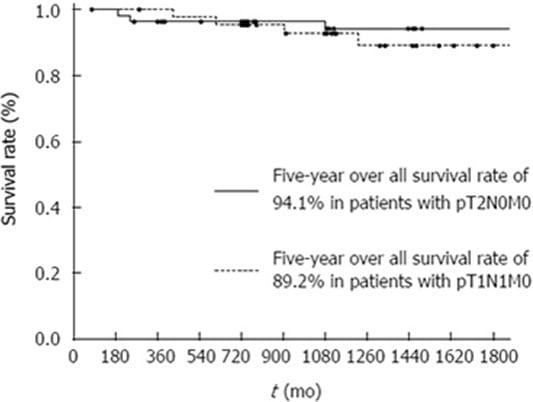
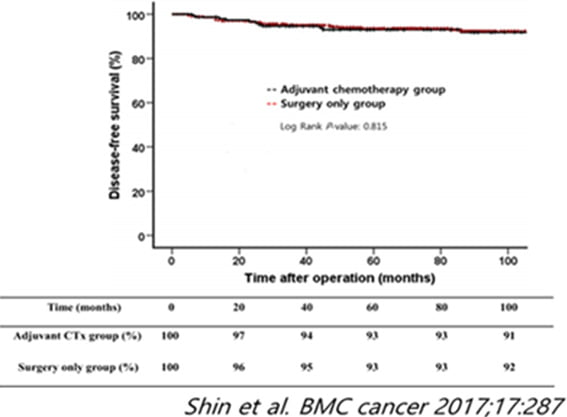
현재 위암 1기 중 림프절 전이가 있는 pT1N1은 현재 표준치료지침이 정립되어 있지 않은 병기로, 각 병원 담당 의사의 개별적인 판단에 근거하여 치료지침이 결정되고 있습니다.
국제 종합 암 네트워크(NCCN: National Comprehensive Cancer Network, Version 3. 2016) (출처: J Natl Compr Cancer Netw. 2016;14:1286-1312) 가이드라인은 같은 IB기 내에서 pT2N0 환자에 비해
pT1N1 환자의 예후가 나쁘기 때문에 항암치료를 권장하고 있습니다. 이에 반해 일본 위암 지침(Japanese Gastric Cancer Treatment Guidelines. Version 4. 2014)에서는 pT1N1 환자에 대해
보조항암요법의 효과가 없다고 보고 있고 (출처: Japanese gastric cancer treatment guidelines 2014), 한국 내 pT1N1 위암 환자 510명을 대상으로 한 분석연구에서도 보조항암요법을 받은 환자와
수술 단독 환자 그룹 사이에 유의한 재발율 차이를 보이지 않았습니다.
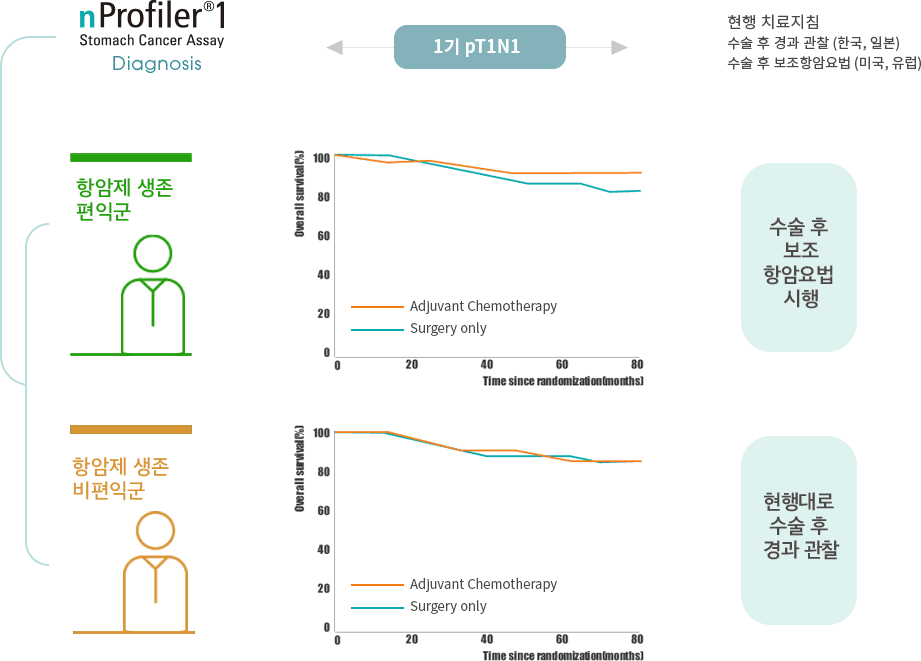
㈜노보믹스는 nProfiler® 1 Stomach Cancer Assay를 이용하여 1기 T1N1 위암 환자에서 재발율이 높은 환자를 선별할 수 있는 연구를 진행하여 2021년 9월 중국암학회 공식 논문인
Chinese Journal of Cancer Research에 그 결과를 발표하였습니다(Chin J Cancer Res 2021;33(5):583-591). 차의과학대학 일산차병원, 세브란스병원, 삼성서울병원 연구진과
㈜노보믹스 공동으로 진행한 연구에 따르면, 1기 위암 환자 중에서 nProfiler® 1 기술 적용으로 고위험군으로 분류된 경우 재발율이 약 10%로 저위험군에서의 2%에 비해 통계적으로 유의하게
재발 가능성이 약 4.4배 높게 나타났습니다.
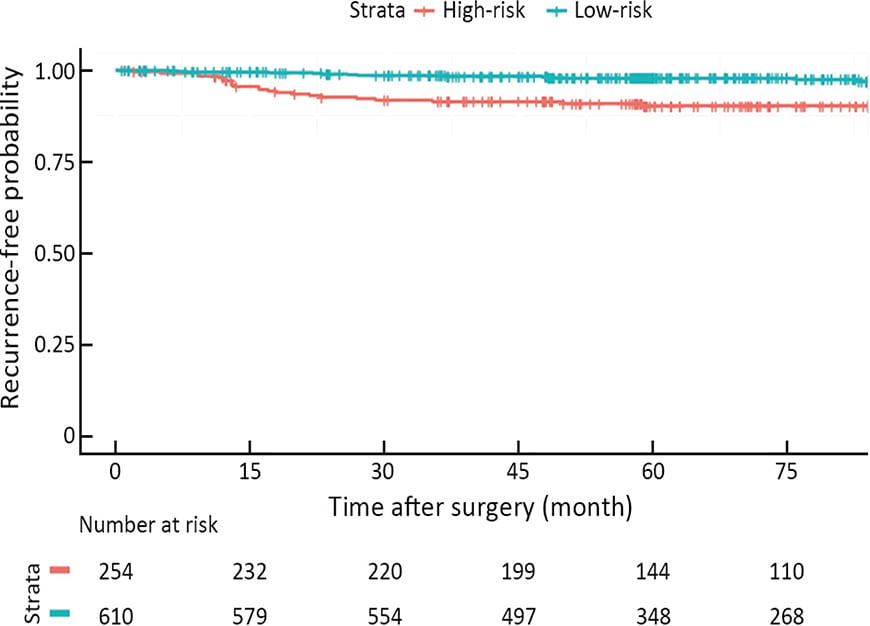
1기 위암도 모두가 완치되는 것이 아니기 때문에 재발 위험에 따른 맞춤형 관리 및 치료가 필요한데, 이번 연구를 통해 그 실현 가능성을 확인하였습니다.
따라서 1기 환자 중 재발율이 높은 고위험군 환자에게는 임상현장에서 수술 후 추가적인 보조항암요법 적용을 고려할 수 있을 것입니다.
 위암 1기 환자의 항암생존편익 효과 예측 검사
위암 1기 환자의 항암생존편익 효과 예측 검사
한국생명공학연구원, 한국기초과학지원연구원, 연세대의과대학 소속의 ㈜노보믹스 대표이사인
허용민 교수 연구팀으로 이루어진 공동 연구진은 위암 분자아형 모사 시스템에서 RSL3 약물이
위암 고위험군의 종양생물학적 특성을 갖는 EMT+ subtype (mesenchymal subtype)위암세포주에
특이적으로 높은 세포사멸 반응을 보이는 것을 확인하였습니다.
본 연구 결과는 지난 2020년 12월에 미국립과학원 ‘PNAS’ 저널에 게재되었습니다.
(PNAS. 2020 Dec 22;117(51):32433-32442)
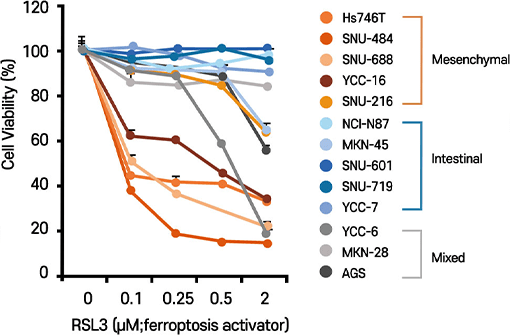
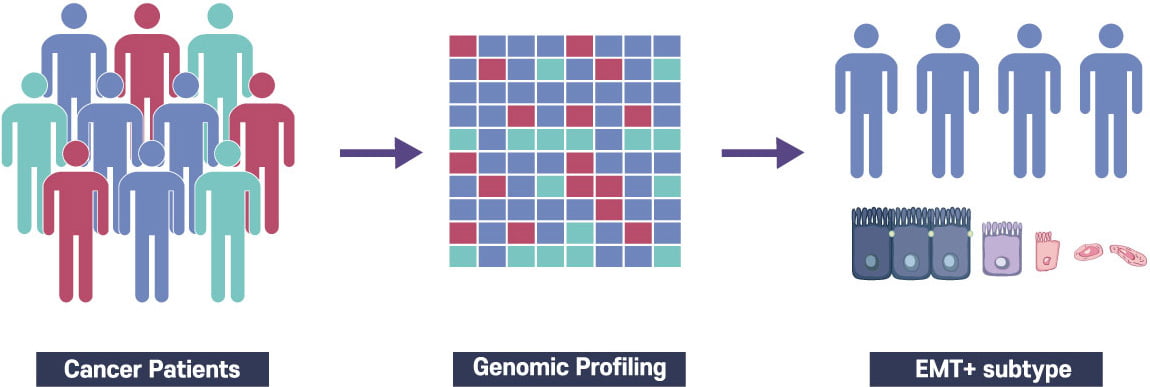
EMT+ subtype (mesenchymal subtype) :㈜노보믹스의 위암예후예측유전자진단 기술에서 밝혀진 가장 예후가 나쁜 환자군으로, 기존 약물에 불응하는 고위험군
RSL3 약물 :현재 전임상 개발 단계에 있는 물질로, 페롭토시스라는 특수한 세포사멸 반응을 유도함
페롭토시스(Ferroptosis) :세포막 지질 성분의 과산화(lipid peroxidation)에 의해 발생하는 세포사멸 경로로 알려져 있음
EMT+ subtype의 분자생물학적 특징 :본 연구에서 상대적으로 지질대사에 관여하는 두 유전자(ELOVL5, FADS1)가 과발현되어 과량으로 축적된 지질대사체로 인해 약물민감도가 증가함을 확인함
더 나아가 페롭토시스 유도 약물 이외도 TGF-β 저해제와 같은 EMT+ subtype (mesenchymal subtype) 환자군에 효과가 있는 약물 연구를 지속하고 있습니다.
TGF-β신호전달 기작은 EMT+ subtype과 상관성이 높다는 연구 결과를 확인하였고, 현재 제약사와 공동으로 고위험군을 대상으로 TGF-β 저해제와 기존 보조항암요법 병행 치료에 대한
임상연구를 시행하고 있습니다.
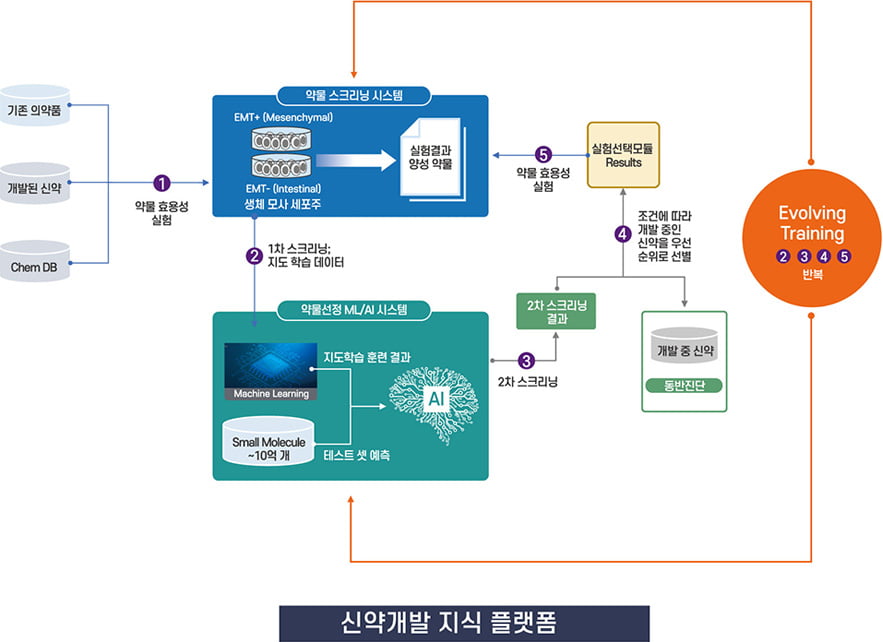
이와 같은 새로운 치료 지침 설계를 위한 신약개발은 ㈜노보믹스 신약개발 지식 플랫폼이 있기 때문에 가능합니다. 신약개발 지식 플랫폼은 인공지능 기반의 지식 플랫폼으로
종양생물학적 특성에 따라 반응하는 후보물질 도출이 가능하여 신약개발에 필요한 시간과 비용을 줄일 수 있습니다. 기존 표준항암치료에 불응하는 난치암의 치료제 개발에
효과적인 신약 개발 모델로, 제약사와 공동연구를 통한 B2B 형태의 동반진단제품 개발이 가능합니다.